UP Board Solutions for Class 10 Science Chapter 4 Carbon and Its Compounds
These Solutions are part of UP Board Solutions for Class 10 Science. Here we have given UP Board Solutions for Class 10 Science Chapter 4 Carbon and Its Compounds.
पाठगत हल प्रश्न
[NCERT IN-TEXT QUESTIONS SOLVED]
खंड 4.1 (पृष्ठ संख्या 68 )
प्रश्न 1.
CO2 सूत्रे वाले कार्बन डाइऑक्साइड की इलेक्ट्रॉन बिंदु संरचना क्या होगी?
उत्तर
CO2 की इलेक्ट्रॉन बिंदु संरचना निम्न आकृति में दर्शाई गई है-

प्रश्न 2.
सल्फ़र के आठ परमाणुओं से बने सल्फर के अणु की इलेक्ट्रॉन बिंदु संरचना क्या होगी? (संकेत- सल्फर के आठ परमाणु एक अँगूठी के रूप में आपस में जुड़े होते हैं।)
उत्तर
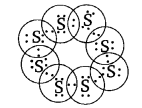
खंड 4.2 ( पृष्ठ संख्या 76)
प्रश्न 1.
पेन्टेन के लिए आप कितने संरचनात्मक समावयवों का चित्रण कर सकते हैं?
उत्तर
पेन्टेन के लिए तीन संरचनात्मक समावयवों का चित्रण संभव है, जिसे निम्न आकृति में दर्शाया गया है-
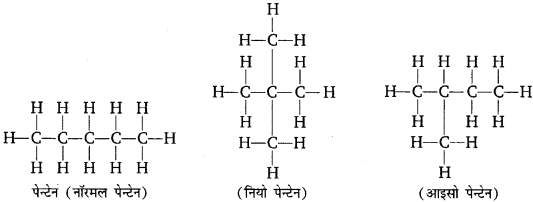
प्रश्न 2.
कार्बन के दो गुणधर्म कौन से हैं, जिनके कारण हमारे चारों कार्बन यौगिकों की विशाल संख्या दिखाई देती है?
उत्तर
कार्बन के वे दो गुणधर्म निम्न हैं, जिनके कारण चारों ओर कार्बन यौगिकों की विशाल संख्या दिखाई देती है-
- श्रृंखलन (Catenation)- कार्बन में कार्बन के दूसरे परमाणुओं के साथ आबंध बनाने की क्षमता होती है जिससे बड़ी संख्या में अणु बनते हैं। इसी गुण के कारण सीधी श्रृंखला, शाखा श्रृंखला तथा वलयाकर श्रृंखला द्वारा बड़ी संख्या में यौगिकों का निर्माण होता है।
- कार्बन की चतुःसंयोजकता- कार्बन की संयोजकता 4 है। इसमें चार अन्य कार्बन परमाणु या ‘कुछ अन्य एक संयोजक तत्वों के परमाणुओं के साथ आबंधन की क्षमता होती है। ऑक्सीजन, हाइड्रोजन, सल्फर, क्लोरीन तथा अनेक अन्य तत्वों के साथ कार्बन के यौगिक बनते हैं। इसके परिणामस्वरूप कार्बन यौगिक की संख्या विशाल होती है|
प्रश्न 3.
साइक्लोपेन्टेन का सूत्र तथा इलेक्ट्रॉन बिंदु संरचना क्या होंगे?
उत्तर
साइक्लोपेन्टेन का सूत्र – C5H10 है। इलेक्ट्रॉन बिंदु संरचना है-

प्रश्न 4.
निम्न यौगिकों की संरचनाएँ चित्रित कीजिए|
(i) एथेनॉइक अम्ल
(ii) ब्रोमोपेन्टेन*
(iii) ब्यूटेनोन
(iv) हेक्सेनैल
*क्या ब्रोमोपेन्टेन के संरचनात्मक समावयव संभव हैं?
उत्तर
1. एथेनॉइक अम्ल (Ethanoic acid) CH3COOH

2. ब्रोमो पेन्टेन (Bromopentane) C5H11Br

3. ब्यूटेनोन (Butanone) C2H5COCH3
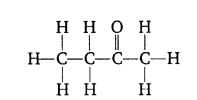
4. हेक्सेनैल (Hexanal) [CH5H11CHO]
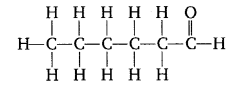
हाँ, ब्रोमोपेन्टेन के संरचनात्मक समावयव संभव हैं जो इस प्रकार हैं-
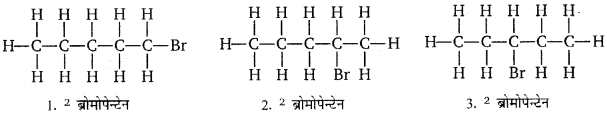
प्रश्न 5.
निम्न यौगिकों का नामकरण कैसे करेंगे?

उत्तर
- ब्रोमो एथेन
- मेथैनल (Methanal)
- 1-हेक्साइन या हेक्साइन
खंड 4.3 (पृष्ठ संख्या 79)
प्रश्न 1.
एथनॉल से एथेनॉइक अम्ल में परिवर्तन को ऑक्सीकरण अभिक्रिया क्यों कहते हैं?
उत्तर
चूँकि क्षारीय पोटैशियम परमैंगनेट (क्षारीय KMnO4) अथवा अम्लीय पोटैशियम डाइक्रोमेट (K2Cr2O7) एथनॉल को एथेनॉइक अम्ल में आक्सीकृत करते हैं अर्थात् ये प्रारंभिक पदार्थ में ऑक्सीजन जोड़ देते हैं, इसलिए इनको ऑक्सीकारक अभिक्रिया कहते हैं।

प्रश्न 2.
ऑक्सीजन तथा एथाइन के मिश्रण का दहन वेल्डिंग के लिए किया जाता है। क्या आप बता सकते हैं कि एथाइन तथा वायु के मिश्रण का उपयोग क्यों नहीं किया जाता?
उत्तर
हम जानते हैं कि वायु में ऑक्सीजन की मात्रा केवल 21% है। अतः ऑक्सीजन की सीमित आपूर्ति के कारण एथाइन का अपूर्ण दहन होता है, जिसके कारण कज्जली ज्वाला (Sooty flame) निकलेगी तथा कम ऊष्मा उत्पन्न होगी। जबकि ऑक्सीजन मिश्रण के साथ पूर्ण दहन के कारण स्वच्छ नीली ज्वाला तथा अधिक ऊष्मा निकलेगी जो धातुओं को गलाकर वेल्डिग करने के लिए आवश्यक ऊष्मा प्रदान करेगी।
खंड 4.4 ( पृष्ठ संख्या 83 )
प्रश्न 1.
प्रयोग द्वारा आप ऐल्कोहॉल एवं कार्बोक्सिलिक अम्ल में कैसे अंतर कर सकते हैं?
उत्तर
- अम्ल का परीक्षण (Acid Test)- दो परखनलियाँ ‘A’ तथा ‘B’ लीजिए। एक में एल्कोहॉल तथा दूसरे में
कार्बोक्सिलिक अम्ल लीजिए। अब दोनों परखनलियों में एक स्पैचुला भरकर NaHCO, या Na2CO3 डालिए। जिस परखनली में तेज़ बुदबुदाहट के साथ CO2 गैस निकलेगी, उसमें अम्ल होंगे। - ऐल्कोहॉल परीक्षण (Alcohol Test)- एक परखनली (A) में 3mL एथेनॉल लेते हैं और 5% क्षारीय पोटैशियम – परमैंगनेट उसमें एक-एक बूंद कर डालते हैं, जल ऊष्मक में गर्म करने पर पोटैशियम परमैंगनेट का रंग गायब हो जाता है, परंतु यही क्रिया एथेनॉइक अम्ल के साथ करने पर रंग अपरिवर्तित रहता है।
प्रश्न 2.
ऑक्सीकारक क्या हैं?
उत्तर
ऑक्सीकारक वे पदार्थ होते हैं, जो ऑक्सीजन प्रदान करते हैं या हाइड्रोजन हटाकर उपचयित करते हैं। जैसे- अम्लीय K2CrO7 तथा क्षारीय KMnO4 ऑक्सीकारक हैं, जो एथेनॉल को ऑक्सीजन प्रदान कर एथेनॉइक अम्ल में बदल देता है। [अभिक्रिया के लिए खंड 4.3, का प्र०-1 देखें।]
खंड 4.5 ( पृष्ठ संख्या 85 )
प्रश्न 1.
क्या आप डिटरजेंट का उपयोग कर बता सकते हैं कि कोई जल कठोर है अथवा नहीं?
उत्तर
नहीं क्योंकि डिटरजेंट (अपमार्जक) कठोर जल एवं मृदु जल दोनों के साथ आसानी से झाग बनाते हैं। अतएव जल की कठोरता की पहचान संभव नहीं होगी।
प्रश्न 2.
लोग विभिन्न प्रकार से कपड़े धोते हैं। सामान्यतः साबुन लगाने के बाद लोग कपड़े को पत्थर पर पटकते हैं, डंडे से पीटते हैं, ब्रुश से रगड़ते हैं या वाशिंग मशीन से कपड़े रगड़े जाते हैं। कपड़ा साफ़ करने के लिए उसे रगड़ने की क्यों आवश्यकता होती है?
उत्तर
साबुन के अणु लंबी श्रृंखला वाले कार्बोक्सिलिक अम्लों के सोडियम एवं पोटैशियम लवण होते हैं। साबुन का आयनिक भाग जल में घुल जाता है, जबकि कार्बन श्रृंखला तेल में घुल जाती है। इस प्रकार साबुन के अणु मिसेली संरचना तैयार करते हैं। अणु का एक सिरा तेल कण की ओर तथा आयनिक सिरा बाहर की ओर होता है, जिसके कारण इमल्शन बनता है। जब कपड़ों को पत्थर पर पटकते हैं, रगड़ते हैं या डंडे से पीटते हैं तो तैलीय या ग्रीज मैल से युक्त मिसेल कपड़ों से हटकर पानी में चंली जाती है। अत: साबुन का मिसेल मैल को पानी में घुलाने में मदद करता है और कपड़े साफ हो जाते हैं।
पाठ्यपुस्तक से हल प्रश्न
[NCERT TEXTBOOK QUESTIONS SOLVED]
प्रश्न 1.
एथेन का आणविक सूत्र-C2H6 है। इसमें-
(a) 6 सहसंयोजक आबंध हैं।
(b) 7 सहसंयोजक आबंध हैं। |
(c) 8 सहसंयोजक आबंध हैं।
(d) 9 सहसंयोजक आबंध हैं।
उत्तर
(b) 7 सहसंयोजक बंधन हैं।
प्रश्न 2.
ब्यूटेनॉन चर्तु-कार्बन यौगिक है, जिसका प्रकार्यात्मक समूह
(a) कार्बोक्सिलिक अम्ल
(b) ऐल्डिहाइड
(C) कीटोन
(d) ऐल्कोहॉल
उत्तर
(C) कीटोन
प्रश्न 3.
खाना बनाते समय यदि बर्तन की तली बाहर से काली हो रही है, तो इसका मतलब है कि
(a) भोजन पूरी तरह नहीं पका है।
(b) ईंधन पूरी तरह से नहीं जल रहा है।
(C) ईंधन आई है।
(d) ईंधन पूरी तरह से जल रहा है।
उत्तर
(b) ईधन पूरी तरह से जल रहा है।
प्रश्न 4.
CH3CI में आबंध निर्माण का उपयोग कर सहसंयोजक आबंध की प्रकृति समझाइए।
उत्तर
CH3CI में तीन एकल बंध कार्बन व हाइड्रोजन परमाणुओं के बीच जुड़े होते हैं और एक एकल बंध कार्बन व क्लोरीन के बीच होता है।
इस तरह कार्बन का अस्टक पूर्ण हो जाता है तथा प्रत्येक हाइड्रोजन के बाहरी कक्ष में भी 2 इलेक्ट्रॉन हो जाते हैं तथा Cl का भी अष्टक पूर्ण हो जाता है। अतः इलेक्ट्रॉनों की साझेदारी द्वारा सहसंयोजक आबंध बनता है।

प्रश्न 5.
इलेक्ट्रॉन बिंदु संरचना बनाइए|
(a) एथेनॉइक अम्ल.
(b) H2S
(C) प्रोपेनोन
(d) F2
उत्तर
(a) एथेनॉइक अम्ल (CH3COOH)
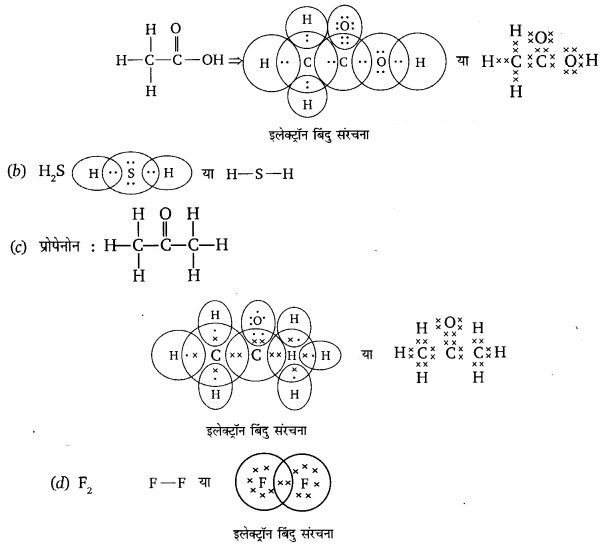
प्रश्न 6.
समजातीय श्रेणी क्या है? उदाहरण के साथ समझाइए।
उत्तर
कार्बनिक यौगिकों की ऐसी श्रेणी जिसकी संरचना तथा रासायनिक गुणों में समानता हो तथा किन्हीं दो लगातार यौगिकों के बीच (-CH2-) इकाई और आणविक द्रव्यमान में 14u का अंतर हो समजातीय श्रेणी कहलाता है।
- समजातीय श्रेणी को एक खास सामान्य सूत्र द्वारा व्यक्त किया जा सकता है।
- इसमें एक ही प्रकार के प्रकार्यात्मक समूह होते हैं; जैसे- CH3OH, C2H5OH, C3H7OH तथा C4H9OH के रासायनिक गुणधर्मों में
अत्यधिक समानता है तथा इनमें (-CH2-) का अंतर है और (-OH) प्रकार्यात्मक समूह हैं। | इन्हें CnH2n+1-OH] सामान्य सूत्र द्वारा व्यक्त किया जा सकता है।
प्रश्न 7.
भौतिक एवं रासायनिक गुणधर्मों के आधार पर एथनॉल एवं एथनॉइक अम्ल में आप कैसे अंतर करेंगे?
उत्तर
(a) भौतिक गुणों में अंतर-

(b) रासायनिक गुणों में अंतर

प्रश्न 8.
जब साबुन को जल में डाला जाता है तो मिसेल का निर्माण क्यों होता है?
उत्तर
साबुन के अणु में दो भाग होते हैं
- लंबी हाइड्रोकार्बन पूँछ → जल विरागी सिरा (Water repelling end) हाइड्रोकार्बन में विलेय
- छोटा आयनिक सिरा → जलरागी सिरा (Water atteracting end)जल में विलेय। जलरागी सिरा

साबुन के अणु साबुन का आयनिक भाग जल में घुल जाता है तथा जल के अंदर होता है, जबकि लंबी हाइड्रोकार्बन पूँछ जल के बाहर होती है। जल के अंदर इन अणुओं की एक विशेष व्यवस्था होती है, जिससे इसका हाइड्रोकार्बन सिरी जल के बाहर बना होता है। ऐसा अणुओं का बड़ा गुच्छा बनने के कारण होता है, जिसमें जलविरागी पूँछ गुच्छे के आंतरिक हिस्से में होती है जबकि उसको आयनिक सिरा गुच्छे की सतह पर होता है। इस संरचना को मिसेल कहते हैं।

प्रश्न 9.
कार्बन एवं उसके यौगिकों का उपयोग अधिकतर अनुप्रयोगों में ईंधन के रूप में क्यों किया जाता है?
उत्तर
कार्बन तथा उसके यौगिकों के दहन पर अत्यधिक मात्रा में ऊष्मा प्राप्त होती है तथा उत्पन्न ऊष्मा को नियंत्रित ढंग से उपयोग किया जा सकता है। इसलिए अधिकतर अनुप्रयोगों के लिए कार्बन तथा इसके यौगिकों को ईंधन के रूप में उपयोग किया जाता है।
प्रश्न 10.
कठोर जल को साबुन से उपचारित करने पर झाग के निर्माण को समझाइए।
उत्तर
कठोर जल में कैल्शियम (Ca2+) तथा मैग्नीशियम (Mg2+) के सल्फेट तथा क्लोराइड के घुलनशील लवण होते हैं, जो साबुन से अभिक्रिया कर अघुलनशील पदार्थ (स्कम) बनाती है। इसी अघुलनशील पदार्थ (स्कम) के कारण झाग आसानी से नहीं बनता है तथा साबुन अधिक मात्रा में उपयोग करना पड़ता है।
कठोर जल + साबुन → स्कम
प्रश्न 11.
यदि आप लिटमस पत्र (लाल एवं नीला) से साबुन की जाँच करें, तो आपका प्रेक्षण क्या होगा?
उत्तर
हम जानते हैं कि साबुन की प्रकृति क्षारीय होती है। अतः लाल लिटमस पत्र को नीला कर देगा।
प्रश्न 12.
हाइड्रोजनीकरण क्या है? इसका औद्योगिक अनुप्रयोग क्या है?
उत्तर
असंतृप्त हाइड्रोकार्बन में पैलेडियम अथवा निकैल जैसे उत्प्रेरकों की उपस्थिति में हाइड्रोजन के योग से संतृप्त हाइड्रोकार्बन बनता है, जिसे हाइड्रोजनीकरण कहते हैं। औद्योगिक अनुप्रयोग – असंतृप्त वसा (वनस्पति तेलों) के हाइड्रोजनीकरण से वनस्पति घी (संतृप्त वसा) बनाया जाता है।

प्रश्न 13.
दिए गए हाइड्रोकार्बन – C2H6 C3H8, C3H6 C2H2 एवं CH4 में किसमें संकलन अभिक्रिया होती है?
उत्तर
दिए गए हाइड्रोकार्बनों में से C3H6तथा C2H2 के साथ संकलन (योग) अभिक्रिया होती है क्योंकि ये असंतृप्त हाइड्रोकार्बन है।

प्रश्न 14.
मक्खन एवं खाना बनाने वाले तेल के बीच रासायनिक अंतर समझने के लिए एक परीक्षण बताइए।
उत्तर
मक्खन एक संतृप्त हाइड्रोकार्बन है जबकि खाना बनाने वाला तेल असंतृप्त हाइड्रोकार्बन है।
परीक्षण-
- ब्रोमीन जल द्वारा–दो अलग-अलग परखनली लेकर एक में तेल तथा दूसरे में मक्खन लीजिए। दोनों परखनलियों |’ में ब्रोमीन जल की कुछ बूंदें डालिए। दोनों परखनलियों को धीरे-धीरे गर्म करने पर हम पाते हैं कि तेल वाले परखनली में ब्रोमीन जल का रंग उड़ जाता है।
- क्षारीय पोटैशियम परमैंगनेट द्वारा-
![]()
प्रश्न 15.
साबुन की सफ़ाई प्रक्रिया की क्रियाविधि समझाइए।।
उत्तर
साबुन के अणु लंबी श्रृंखला वाले वसीय अम्लों के सोडियम लवण होते हैं, जिसमें दो भाग होते हैं- लंबी हाइड्रोकार्बन पूँछ तथा छोटी आयनिक सिरा। उदाहरण के लिए-
C15H31COONa, C17H33COONa आदि
इसे हम निम्न प्रकार भी दर्शाते हैं-

जब पानी में साबुन घोला जाता है, तब जलरागी सिरा जल में घुलनशील तथा जल विरागी सिरा जल में अघुलनशील परंतु तैलीय मैल, वसा इत्यादि में घुलनशील होते हैं। किसी कपड़े या वस्तु पर साबुन के अणु इस प्रकार व्यवस्थित हो जाते हैं कि इनका आयनिक सिरा जल के अंदर तथा हाइड्रोकार्बन पूँछ जल के बाहर होती है। ऐसा अणुओं का बेड़ा गुच्छा बनने के कारण होता है, जिसमें जल विरागी पूँछ गुच्छे के आंतरिक हिस्से में होती है, जबकि उसका आयनिक सिरा गुच्छे की सतह पर होता है। इस संरचना को मिसेल कहते हैं। तैलीय मैल मिसेल के केन्द्र में एकत्र हो जाता है। मिसेल विलयन में कोलॉइड के रूप में बना रहता है तथा आयन-आयन विकर्षण के कारण वह अवक्षेपित नहीं होता। अतः मिसेल में तैरता मैल रगड़ कर यो डंडे से पीटकर आसानी से हटाया जा सकता है। [देखिए चित्र (4.4)]
Hope given UP Board Solutions for Class 10 Science Chapter 4 are helpful to complete your homework.